Kontak:Salah Zhou (Tn.)
Telp: ditambah 86-551-65523315
Seluler/WhatsApp: ditambah 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Surel:sales@homesunshinepharma.com
Menambahkan:1002, Huanmao Bangunan, No.105, Mengcheng Jalan, Hefei Kota, 230061, Cina
Mitra Zai Lab argenx baru-baru ini mengumumkan bahwa European Medicines Agency (EMA) telah menerima aplikasi otorisasi pemasaran (MAA) untuk efgartigimod, antagonis FcRn untuk pengobatan miastenia gravis sistemik (gMG). EMA telah memulai proses peninjauan formal dan diharapkan membuat keputusan peninjauan pada pertengahan 2022. Saat ini, pengobatan gMG efgartigimod' juga sedang ditinjau oleh FDA AS, dan tanggal target Undang-Undang Biaya Pengguna Obat Resep (PDUFA) adalah 17 Desember 2021. Awal tahun ini, argenza juga mengajukan aplikasi untuk efgartigimod untuk mengobati gMG ke Badan Farmasi dan Alat Kesehatan Jepang (PMDA).
Miastenia gravis (MG) adalah penyakit neuromuskular yang diperantarai oleh IgG patogen dan secara serius mempengaruhi kualitas hidup. Gejala penyakit dan efek samping dari terapi saat ini dapat menyebabkan kerusakan signifikan pada kehidupan pasien. MG dapat berdampak buruk pada kehidupan dan kemandirian pasien' dan dapat mempengaruhi kemampuan menelan, berbicara, berjalan, dan bahkan bernapas. Selain itu, setiap pasien mengalami MG berbeda, yang membuat manajemen penyakit tidak dapat diprediksi.
Jika disetujui, efgartigimod akan menjadi antagonis FcRn pertama dan satu-satunya yang menerima persetujuan regulator dan akan memberikan terapi bertarget pertama untuk pasien gMG. Hasil dari uji coba ADAPT Fase 3 yang sangat penting menunjukkan bahwa pengobatan efgartigimod dapat secara signifikan meningkatkan kekuatan dan kualitas hidup pasien dengan gMG. Secara khusus, sebagian besar pasien yang diobati dengan efgartigimod telah mengamati perbaikan klinis yang signifikan dalam 2 minggu pertama pemberian. Hasil ini memiliki implikasi penting bagi komunitas MG.
Penerapan regulasi efgartigimod untuk pengobatan gMG didasarkan pada hasil uji coba ADAPT Fase 3 yang sangat penting. Data yang relevan diterbitkan di The Lancet Neurology pada bulan Juni tahun ini. Judul artikel adalah: Keamanan, kemanjuran, dan tolerabilitas efgartigimod pada pasien dengan generalized myasthenia gravis (ADAPT): uji coba fase 3 multisenter, acak, terkontrol plasebo.
Hasil penelitian menunjukkan bahwa uji coba ADAPT mencapai titik akhir primer: pada pasien dengan antibodi reseptor asetilkolin positif (AChR Ab+) gMG, menurut skor aktivitas kehidupan sehari-hari (MG-ADL) miastenia gravis, dibandingkan dengan plasebo kelompok, kelompok perlakuan efgartigimod memiliki lebih banyak. Sebagian besar pasien adalah responden (67,7% vs 29,7%; p<0,0001). responden="" didefinisikan="" memiliki="" peningkatan="" minimal="" 2="" poin="" dalam="" skor="" mg-adl="" selama="" 4="" minggu="" berturut-turut="" atau="" lebih="" lama.="" selain="" itu,="" 40%="" pasien="" dalam="" kelompok="" pengobatan="" efgartigimod="" mencapai="" ekspresi="" gejala="" minimal="" (didefinisikan="" sebagai="" skor="" mg-adl="" 0="" [asimptomatik]="" atau="" 1),="" sedangkan="" proporsi="" pasien="" dalam="" kelompok="" plasebo="" yang="" mencapai="" tujuan="" ini="" hanya="" 11,1%.="" di="" antara="" responden="" achr-ab+,="" 84,1%="" pasien="" mengalami="" peningkatan="" skor="" mg-adl="" yang="" signifikan="" secara="" klinis="" dalam="" 2="" minggu="" pertama="" pengobatan.="" dalam="" penelitian="" ini,="" keamanan="" efgartigimod="" sebanding="" dengan="">
Setelah menyelesaikan uji coba ADAPT, 90% pasien mengikuti uji coba ADAPT plus, sebuah studi ekstensi label terbuka yang berlangsung selama 3 tahun untuk mengevaluasi keamanan jangka panjang dan tolerabilitas efgartigmod. Dalam ADAPT dan ADAPT plus, setidaknya 118 pasien menerima pengobatan efgartigmod selama 12 bulan atau lebih.
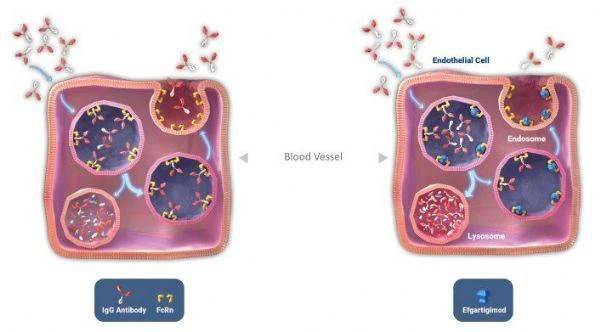
mekanisme aksi efgartigimod
Efgartigimod adalah fragmen antibodi yang sedang dikembangkan, dirancang untuk mengurangi antibodi imunoglobulin G (IgG) patogen dan memblokir sirkulasi IgG. Efgartigimod dapat mengikat FcRn, yang diekspresikan secara luas di seluruh tubuh dan memainkan peran sentral dalam mencegah degradasi antibodi IgG. Memblokir FcRn dapat mengurangi tingkat ekspresi antibodi IgG dan dapat mengobati penyakit autoimun yang diketahui didorong oleh antibodi IgG patogen, termasuk: myasthenia gravis (MG), penyakit kronis yang menyebabkan kelemahan otot; pemfigus vulgaris ( PV), penyakit kulit kronis yang ditandai dengan kulit melepuh parah; trombositopenia imun (ITP), penyakit kronis yang dimanifestasikan oleh ekimosis dan perdarahan; polineuropati demielinasi inflamasi kronis (CIDP) ), penyakit di mana kerusakan pada sistem saraf menyebabkan gangguan gerakan.
Pada tanggal 6 Januari 2021, Zai Lab dan argenx mengumumkan bahwa kedua pihak telah mencapai kerjasama resmi yang eksklusif, dan Zai Lab akan bertanggung jawab untuk memajukan pengembangan dan komersialisasi efgartigimod di Tiongkok Raya (termasuk Tiongkok Daratan, Hong Kong, Taiwan, dan Makau ) .
Dr Ren Hairui, kepala petugas medis di bidang autoimunitas dan anti-infeksi dari Zai Lab, mengatakan: Saat ini ada sekitar 200.000 pasien dengan myasthenia gravis di China. Pilihan pengobatan yang ada sangat terbatas dan ada banyak kebutuhan klinis yang belum terpenuhi. Berdasarkan data efgartigimod yang ada, produk ini diharapkan dapat mengubah status pengobatan miastenia gravis sistemik saat ini dan penyakit autoimun serius lainnya setelah disetujui.
Menurut ketentuan perjanjian, Zai Lab akan mendapatkan hak eksklusif untuk mengembangkan dan mengkomersialkan efgartigimod di Tiongkok Raya. Zai Lab akan bertanggung jawab atas penelitian klinis pendaftaran global dan pengembangan efgartigimod untuk berbagai indikasi di Cina. Selain itu, Zai Lab juga akan bertanggung jawab untuk memulai studi konfirmasi fase 2 untuk beberapa indikasi baru di Tiongkok Raya guna mempercepat pengembangan lebih banyak indikasi autoimun untuk efgartigimod dalam skala global.