Kontak:Salah Zhou (Tn.)
Telp: ditambah 86-551-65523315
Seluler/WhatsApp: ditambah 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Surel:sales@homesunshinepharma.com
Menambahkan:1002, Huanmao Bangunan, No.105, Mengcheng Jalan, Hefei Kota, 230061, Cina
Perusahaan biofarmasi Merck KGaA&# 39 EMD Serono baru-baru ini merilis data efikasi dan keamanan jangka panjang untuk oral, penghambat BTK evobrutinib yang sangat selektif dalam perawatan pasien dewasa dengan kekambuhan sklerosis multipel (RMS). Hasil ini dari studi Open Label Extension (OLE) Tahap II.
Data terbaru menunjukkan bahwa evobrutinib adalah inhibitor BTK pertama yang melaporkan kemanjuran dan keamanan data hingga 108 minggu dalam pengobatan MS. evobrutinib adalah inhibitor BTK pertama dan satu-satunya yang menunjukkan kemanjuran tinggi selama 108 minggu. Tidak ada sinyal keamanan baru selama periode perpanjangan label terbuka (OLE) selama 60 minggu, yang konsisten dengan data dari 1, 200 pasien dengan MS atau penyakit lain yang telah diobati dengan evobrutinib hingga saat ini. .
Luciano Rossetti, kepala global RGG amp; D di Merck Serono, mengatakan:" Data ini menunjukkan bahwa evobrutinib memiliki dampak berkelanjutan dan sangat tinggi pada tingkat kekambuhan tahunan dalam 108 minggu perawatan. Kemanjuran maksimum jelas terkait dengan jejak BTK, yang selanjutnya memvalidasi pilihan dosis kami untuk fase program ini. Kami juga didorong oleh data keselamatan yang luas dan konsisten dari evoburtinib, termasuk tidak ada peningkatan infeksi serius pada lebih dari 1, 200 pasien dalam 2 tahun."
Hasil tingkat kambuh tahunan (ARR) dari periode double-blind penelitian tetap tidak berubah selama periode ekstensi label terbuka. Pasien yang menerima evobrutinib 75 mg BID (dua kali sehari) selama periode double-blind memiliki ARR 0. 11 (95% CI) pada minggu 48 : 0. 04 - 0. 25), ARR pada minggu 108 adalah 0. 12 (95% CI: 0. 06 –0. 22).
Data dari studi Fase II terus membuktikan bahwa rejimen dosis BID lebih efektif daripada rejimen dosis QD (sekali sehari) dalam hasil klinis, sebagaimana dibuktikan dengan pengurangan ARR. Data pemodelan menunjukkan bahwa pada hampir semua pasien, tingkat hunian BTK bawah harus lebih besar dari 95% untuk mencapai kemanjuran tertinggi, dan rejimen dosis BID dapat mencapai efek ini dengan baik.
Data yang sebelumnya diterbitkan dalam New England Journal of Medicine (NEJM) melaporkan hasil penelitian fase II: pada minggu 24, evobrutinib secara signifikan mengurangi jumlah kumulatif lesi yang ditingkatkan T1-Gd, mencapai ujung utama. Pada minggu 48, semua pasien dapat memasuki periode perpanjangan label terbuka (OLE) untuk mengevaluasi efikasi jangka panjang dan keamanan evobrutinib.
Xavier Montalban, Ketua dan Direktur Departemen Neuroimunologi dan Departemen Neurorehabilitasi Catalonia Multiple Sclerosis Center (Cemcat) di Rumah Sakit Universitas Valde Hebron di Barcelona, Spanyol, mengatakan:" Keefektifan dan keamanan dari 108 minggu dari seluruh periode double-blind dan periode OLE Data seksual sangat kuat. Hasil ini, dikombinasikan dengan selektivitas tinggi, menunjukkan bahwa evobrutinib memiliki potensi untuk memberikan pengobatan yang sangat menjanjikan untuk MS."
Dari 267 pasien yang diacak, 213 pasien menyelesaikan 108 minggu pengobatan (48 minggu dalam studi utama dan 60 minggu di OLE). Evobrutinib umumnya ditoleransi dengan baik dan menjaga keamanan yang konsisten selama OLE, termasuk tidak ada peningkatan infeksi, dan secara keseluruhan tidak ada sinyal keselamatan baru yang ditemukan. Konsisten dengan selektivitas tinggi evobrutinib, pasien yang berpartisipasi dalam uji coba tidak mengalami efek samping sistemik seperti gangguan pencernaan. Dalam uji coba fase II, reaksi merugikan paling umum dari setiap tingkatan yang terkait dengan evobrutinib termasuk nasofaringitis dan peningkatan kadar alanine aminotransferase (ALT), aspartate aminotransferase (AST), dan lipase.
Peningkatan sementara transaminase hati terbatas pada minggu pertama 24 setelah memulai pengobatan evobrutinib, dan tidak diamati pada pasien yang terus menggunakan pengobatan evobrutinib selama fase OLE.
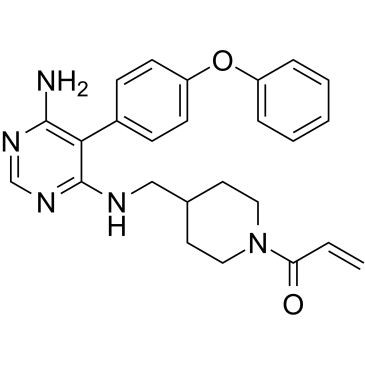
rumus struktur kimia evobrutinib (Sumber: medchemexpress.cn)
Setelah mencapai titik akhir primer pada minggu ke 24 pengobatan dalam studi fase II, evobrutinib memasuki fase III pengembangan klinis. Dua uji coba baru EVOLUTION RMS 1 dan 2 adalah multisenter, acak, kelompok paralel, uji coba ganda terkontrol, simulasi ganda, kontrol obat positif, dilakukan pada pasien RMS, titik akhir utama masing-masing percobaan adalah ARR pasien setelah 96 minggu pengobatan. Titik akhir sekunder termasuk penampilan lesi T 2 baru atau yang diperbesar yang dinilai dengan pemindaian MRI, dan kecacatan progresif yang diukur dengan Skala Status Cacat yang Diperpanjang (EDSS).
Multiple sclerosis (MS) adalah penyakit sistem saraf pusat inflamasi kronis dan penyakit neurologis non-invasif yang paling umum menyerang pada orang muda. Diperkirakan sekitar 2. 3 juta orang di seluruh dunia menderita multiple sclerosis. Meskipun gejala dapat bervariasi, gejala MS yang paling umum termasuk penglihatan kabur, mati rasa atau kesemutan pada anggota badan, dan masalah kekuatan dan koordinasi. Jenis kekambuhan multiple sclerosis adalah yang paling umum.
Evobrutinib (M 2951) saat ini sedang dalam pengembangan klinis untuk mengeksplorasi potensinya sebagai pengobatan untuk multiple sclerosis (MS). Obat ini adalah inhibitor Bruton tyrosine kinase (BTK) oral, sangat selektif. BTK memainkan peran penting dalam pengembangan dan fungsi berbagai sel imun termasuk limfosit B dan makrofag.
evobrutinib dirancang untuk menghambat respon sel B utama, seperti proliferasi, antibodi dan pelepasan sitokin, tanpa secara langsung mempengaruhi sel T. Penghambatan BTK diyakini menghambat sel-sel yang memproduksi autoantibodi. Studi praklinis telah menunjukkan bahwa penghambatan BTK mungkin memiliki efek terapi pada penyakit autoimun tertentu. Saat ini, proyek pengembangan klinis fase III global sedang mengevaluasi evobrutinib untuk MS. Proyek ini mencakup dua studi kunci fase III, EVOLUTION RMS 1 dan 2. evobrutinib saat ini dalam pengembangan klinis dan belum disetujui oleh negara mana pun.